|
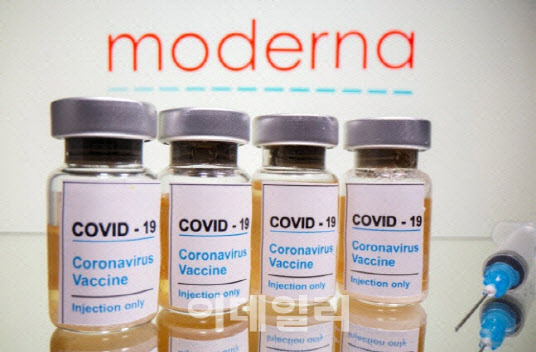
식품의약품안전처는 GC녹십자의 ‘모더나코비드-19백신주’의 임상결과에 대해 두번째 전문가 자문 절차인 중앙약사심의위원회를 열었다고 13일 밝혔다.
식약처는 코로나19 치료제와 백신의 객관적이고 투명한 허가·심사를 위해 ‘3중’ 자문 절차를 진행하고 있다. 전문가 자문은 검증 자문단, 중앙약사심의위원회, 최종점검위원회 순서로 진행된다.
중앙약심의위원회는 1차 검증 때와 마찬가지로 모더나 백신의 예방 효과에 대해 18세 이상 2회 투여 14일 후 효과가 확인되기 때문에 허가를 위한 예방효과는 인정가능하다고 판단했다.
중앙약심의위원회는 모더나 백신의 안전성에 대해서도 허용할 만한 수준이라고 봤다. 다만, 국내에서 허가된 코로나19 mRNA 백신과 같이 2차 투여 후 더 많은 통증, 피로, 오한 등 접종에 의한 예측되는 사례 발생 증가 경향이 있어 안내가 필요하다고 자문했다.
식약처는 모더나 백신의 품질자료 등 최종 점검에 필요한 추가 제출자료를 검토한 후 ‘최종점검위원회’를 개최해 허가 여부를 최종 결정할 예정이다. 식약처는 구체적인 3차 자문 절차 일정을 공개하지는 않았다.
국내 허가 제품은 영하 25∼영하 15℃에서 7개월, 냉장 상태인 2∼8℃에서 1개월 보관, 상온 수준인 8∼25℃ 사이에는 12시간 보관할 수 있는 조건으로 허가가 신청됐다. 1바이알(약병) 당 10명 접종할 수 있다. 국내에서는 GC녹십자가 모더나 백신 허가와 유통을 맡고 있다.

![월드컵까지 따냈다...스포츠산업 '생태계 파괴자' 된 빈살만[글로벌스트롱맨]](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/11/PS23110500115t.jpg)

![[포토] 폭염 속 휴식취하는 건설 근로자](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/08/PS23080100718t.jpg)






![[포토]최은우 '선두가 보인다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900548t.jpg)
![[포토] 통합방위 발언하는 서강석 송파구청장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900809t.jpg)
![[포토]청년도약계좌 22일부터 가입신청](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900757t.jpg)
![[포토] "의대 총장들 건의 수용한다"](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900703t.jpg)
![[포토] 학생들과 기념촬영하는 이재명](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900584t.jpg)
![[포토]김윤혜, 인형 그 자체](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900148t.jpg)
![[포토] 고군택 '이번주 우승은 제가 하겠습니다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900241t.jpg)


![[포토]유정복 인천시장 축사](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041800929t.jpg)
![[포토]송민교 '버디를 노려본다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042000015t.jpg)