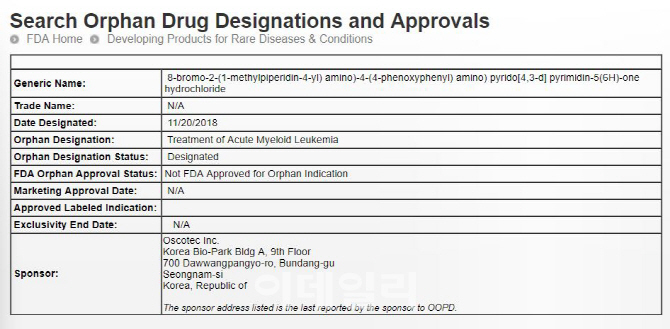
 | | 오스코텍의 백혈병치료제 ‘SKI-G801’의 희귀의약품 지정 내용이 담긴 미국 식품의약국(FDA) 안내문.(자료=FDA) |
|
[이데일리 김지섭 기자] 바이오벤처인
오스코텍(039200)이 미국에서 희귀의약품 지정 허가를 받았다. 이 회사는
유한양행(000100)이 최근 12억 5500만달러(약 1조4030억원)에 기술수출한 표적항암제 ‘레이저티닙’을 발굴한 업체다.
21일 업계에 따르면 미국 식품의약국(FDA)은 지난 20일(현지시간) 오스코텍이 개발하고 있는 급성 골수성 백혈병치료제 ‘SKI-G801’을 희귀의약품으로 지정했다. SKI-G801는 급성 백혈병 치료제로 미국에서 전임상(동물실험)을 완료하고 지난해 12월부터 임상 1상을 진행하고 있다.
만성골수성백혈병은 ‘글리벡’이라는 표적치료제가 등장해 10년 이상 생존률이 80~90%에 달하지만, 급성골수성백혈병은 현재 완벽한 치료제가 없다. 같은 계열(FLT3 저해제)에서 이미 상용화된 제품은 스위스 노바티스의 ‘PKC-412’가 있고, 일본 다케다의 TAK-659 등이 임상을 진행하고 있지만 오스코텍이 개발하고 있는 SKI-G801은 동물실험에서 효과가 기존 제품보다 오래 유지되는 것으로 확인됐다. 계열내최고(베스트인클래스) 의약품 출시를 노릴 수 있는 위치에 있는 것이다.
이에 FDA가 이번에 SKI-G801의 희귀의약품 지정을 승인한 것으로 풀이된다. FDA는 지난 1983년 제정한 ‘희귀의약품법’에 따라 희귀난치성 질병이나 생명을 위협하는 질병을 치료하는 약의 경우 희귀의약품으로 지정한다. 환자 수가 20만명을 넘지 않거나, 이를 넘더라도 제약사가 시장성이 없어 개발하지 않을 것 같은 질환을 대상으로 한다. FDA로부터 희귀의약품으로 지정되면 △7년간 독점권 인정 △개발비 세액공제 △품목허가 신청 시 수수료 면제 등의 혜택이 있다. 일반적인 신약(5년)보다 독점 기간이 길고 허가 과정에서 각종 경제적 혜택을 받을 수 있는 것이다.
이번 희귀의약품 지정에 따라 SKI-G801은 향후 상업화에도 속도를 낼 것으로 기대된다. 오스코텍 김중호 전무는 “SKI-G801이 약효를 확인하고 기술적으로 인정을 받았기 때문에 FDA로부터 희귀의약품 지정을 받은 것”이라며 “희귀의약품 지정에 따른 혜택이 기대된다”고 말했다.
 | | 오스코텍 CI(자료=오스코텍) |
|

![월드컵까지 따냈다...스포츠산업 '생태계 파괴자' 된 빈살만[글로벌스트롱맨]](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/11/PS23110500115t.jpg)

![[포토] 폭염 속 휴식취하는 건설 근로자](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/08/PS23080100718t.jpg)








![[포토]최은우 '선두가 보인다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900548t.jpg)
![[포토] 통합방위 발언하는 서강석 송파구청장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900809t.jpg)
![[포토]청년도약계좌 22일부터 가입신청](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900757t.jpg)
![[포토] "의대 총장들 건의 수용한다"](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900703t.jpg)
![[포토] 학생들과 기념촬영하는 이재명](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900584t.jpg)
![[포토]김윤혜, 인형 그 자체](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900148t.jpg)
![[포토] 고군택 '이번주 우승은 제가 하겠습니다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900241t.jpg)


![[포토]유정복 인천시장 축사](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041800929t.jpg)
!['더 뉴 아이오닉5'…"디자인·편의성·승차감 다 좋아졌네"[타봤어요]](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900771t.jpg)
![[포토]송민교 '버디를 노려본다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042000015t.jpg)