|
화이자와 바이오엔테크는 이날 5~11세 어린이 2268명을 대상으로 한 코로나19 백신 임상시험 자료를 미 식품의약국(FDA)에 제출했다고 밝혔다. 그러면서 향후 몇 주 이내에 어린이용 백신에 대해 긴급사용 승인을 공식 신청할 계획이라고 덧붙였다.
당초 화이자 측은 이달 말까지 신청서를 제출한다는 목표였다. 이에 학부모, 공중보건 및 백신 전문가 등은 다음 달에 5~11세 어린이들에게도 백신을 접종할 수 있을 것으로 기대했다. 그러나 임상데이터 제출이 늦어지면서 긴급사용 승인 신청도 미뤄지게 됐고, 미 보건당국의 승인도 지연될 전망이다.
해당 사안에 정통한 소식통은 WSJ에 “화이자는 10월 중순까지 어린이용 백신 긴급사용 승인을 신청하지 못할 수 있다. 이는 FDA가 할로윈데이(10월 31일)부터 추수감사절(11월 25일) 사이 어느 시점에 결정을 내리지 못할 수 있음을 의미한다”고 말했다.
앞서 FDA는 “12세 미만 어린이들이 백신을 맞을 수 있도록 24시간 내내 노력하고 있지만, (엄격한) 테스트와 규제 절차가 필요하다”며 조심스러운 입장을 내비쳤다.
한편 화이자가 이날 제출한 임상시험 자료에는 12세 미만 어린이들에게도 백신 효과가 긍정적이라는 내용이 담겼다.
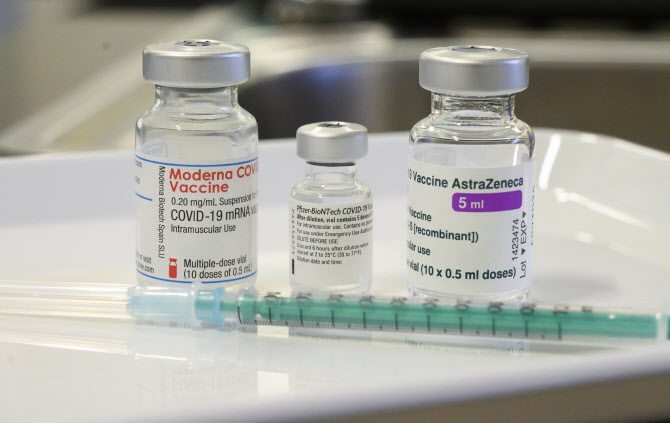
화이자-바이오엔테크는 5~11세 어린이 2268명에게 성인·청소년 기준 투여량의 3분의 1인 10㎍(마이크로그램)의 백신을 3주 간격으로 2회 투여하는 시험을 진행했다. 그 결과 12세 이상과 마찬가지로 안전하고 강력한 항체를 생성하는 것으로 나타났다.
화이자-바이오엔테크는 유럽연합(EU) 등 다른 국가 보건당국에도 이 자료를 제공할 방침이다. 아울러 생후 6개월~2세 영유아에 대한 임상시험 결과는 올해 4분기에 나올 예정이라고 예상했다.

![월드컵까지 따냈다...스포츠산업 '생태계 파괴자' 된 빈살만[글로벌스트롱맨]](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/11/PS23110500115t.jpg)

![[포토] 폭염 속 휴식취하는 건설 근로자](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/08/PS23080100718t.jpg)






![[포토] 의대정원 논의되는 중앙재난안전대책본부 회의](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900621t.jpg)
![[포토] 이주호 교육부 장관과 조규홍 보건복지부 장관의 대화](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900618t.jpg)
![[포토] 학생들과 기념촬영하는 이재명](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900584t.jpg)
![[포토]김윤혜, 인형 그 자체](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900148t.jpg)
![[포토] 타구 살피는 이창우](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900063t.jpg)


![[포토]유정복 인천시장 축사](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041800929t.jpg)
![[포토] 고군택 '신들린 샷으로 초대 챔피언을 노린다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041800207t.jpg)
![[포토]제60회 한국보도사진전 찾은 유인촌-오세훈](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041800649t.jpg)
![[포토] 아들 바보 허인회](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24041900205t.jpg)
