[이데일리 왕해나 기자]식품의약품안전처는 국내에서 개발한 코로나19 백신 2종의 임상 1/2상 시험 계획을 승인했다고 4일 밝혔다. 이번에 승인받은 국산 백신 2종은 셀리드의 ‘AdCLD-CoV19’과 진원생명과학의 ‘GLS-5310’이다.
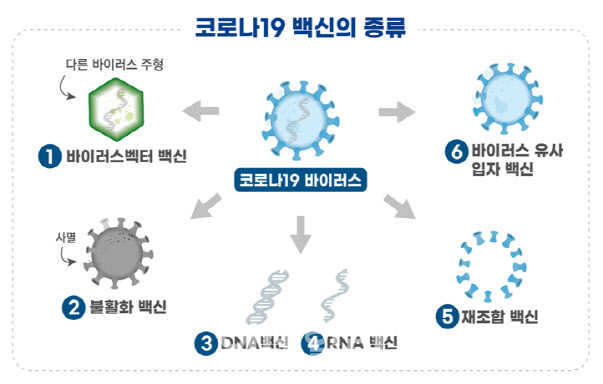 | | 방식별 코로나19 백신 종류. (그림=식약처) |
|
셀리드의 AdCLD-CoV19 후보물질에 대한 임상시험은 건강한 성인을 대상으로 해당 백신의 안전성 및 면역원성을 평가하기 위한 1/2상 임상시험이다. 셀리드의 백신은 코로나19 표면항원 유전자를 아데노 바이러스 주형에 넣어 제조한 바이러스벡터 백신이다. 아데노 바이러스 주형을 통해 사람 세포 내로 전달된 표면항원 유전자가 체내에서 표면항원 단백질을 합성해 중화항체 생성을 유도하고, 이후 코로나19가 침입했을 때 이 중화항체가 코로나19를 제거하는 방식이다. 영국 아스트라제네카, 중국 캔시노사, 러시아 가말레야연구소, 미국 존슨앤드존슨이 바이러스벡터 백신을 개발하고 있다.
진원생명과학의 GLS-5310 후보물질 임상시험은 건강한 성인을 대상으로 해당 백신의 안전성 및 면역원성을 평가하기 위한 1·2상 임상시험이다. 이 백신은 코로나19의 표면항원 유전자를 플라스미드(DNA) 형태로 제조한 DNA 백신이다. DNA백신 예방원리는 접종한 코로나19 표면항원 유전자에 의해 체내에서 표면항원 단백질을 합성해 중화항체 생성을 유도하고, 이후 코로나19가 침입했을 때 이 중화항체가 코로나19를 제거한다. 국내 제넥신, 미국 이노비오가 DNA 백신을 개발하고 있다.
식약처는 “안전하고 효과 있는 코로나19 치료제·백신이 신속히 개발될 수 있도록 필요한 사항을 지원해 우리 국민이 치료 기회를 보장받을 수 있도록 최선을 다할 계획”이라고 말했다.