|
14일 식품의약품안전처에 따르면, 렉키로나는 임상 3상 결과를 올해 연말까지 제출하는 조건으로 조건부 허가를 받았다. 이에 따라 임상 3상 결과를 기한 내 내놓지 못하거나 결과가 좋지 않으면 허가가 취소될 수 있는 상황이다. 임상의 성패 여부는 허가 당국의 판단에 달려있지만, 통상 1차 유효성 지표로 평가한다.
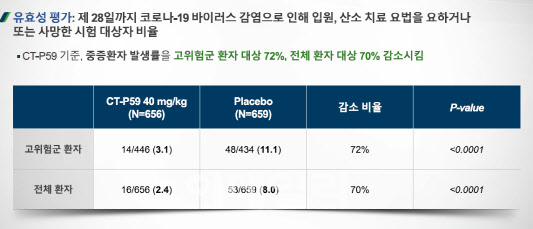
셀트리온은 이날 임상 3상 결과 발표에서 1차 유효성 지표로 ‘고위험군 환자의 중증 악화율’을 설정했다고 밝혔다. 고위험군 환자에게 렉키로나를 투여했을 때 그렇지 않은 경우보다 입원 및 산소치료를 요하는 상태로 악화하거나 사망하는 환자의 비율을 얼마나 줄이느냐를 봤다는 것이다. 임상 결과, 렉키로나 투약군은 위약군 대비 중증 악화율을 72% 줄였고 통계적 유의성(P밸류)도 만족시켰다. 통계적 유의성을 달성했다는 것은 셀트리온 임상 3상 결과가 우연이나 실수에 의해 나온 게 아니라 신뢰할 만하다는 의미다.
원활한 수출을 위해서는 렉키로나가 변이 바이러스에 대한 효과까지 입증해야 한다는 지적도 나온다. 이재갑 교수는 “렉키로나는 남아공 변이에 대해서는 효과가 떨어질 것으로 예상되고 있어 그 부분에 대해 보완을 해야 할 것 같다”며 “미국 식품의약국(FDA)은 단독 치료제에 대해 의구심을 표하고 있어 변이에 대한 부분을 어떻게 준비하느냐가 중요할 것”이라고 강조했다. 이날 셀트리온 관계자는 “임상을 할 때 변이를 고려해서 진행한 부분은 제한적”이라며 “환자가 들어왔을 때 어떤 변이인지 파악하는 게 원할하지 않다. 주요 지표 발표 이후 7월 중에 (임상 군에) 어떤 변이 분포를 가졌는지 데이터가 나오면 볼 수 있을 것 같다”고 말했다.


![월드컵까지 따냈다...스포츠산업 '생태계 파괴자' 된 빈살만[글로벌스트롱맨]](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/11/PS23110500115t.jpg)

![[포토] 폭염 속 휴식취하는 건설 근로자](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/08/PS23080100718t.jpg)






![[포토]코스피, 질주하는 테슬라 증시 훈풍](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000818t.jpg)
![[포토] 꽃처럼 아름다워](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000766t.jpg)
![[포토]국방 AI정책방향 소개하는 이영빈 기획조정실장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000623t.jpg)
![[포토]'빅5병원' 오늘 외래·수술 셧다운… 의료대란 현실화되나](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000540t.jpg)
![[포토]인사 나누는 방재승 비대위원장-안철수 의원](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000519t.jpg)
![[포토]에릭 AI Tech Collaboration 담당, 텔코 LLM 소개](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000474t.jpg)
![[포토]국군장병 취업박람회 인재 채용](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900871t.jpg)
![[포토]멘토들 강연 경청하는 오세훈 시장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900762t.jpg)
![[포토]KT그룹, AI로 미디어·콘텐츠 산업 '가속도'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900526t.jpg)
![[포토] 한우자조금, "한우로 행복하세요~"](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900479t.jpg)
![[포토] 임성재의 우승 본능](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042800425t.jpg)
![[르포]'청정 제주'서 만나는 전기차·UAM…미래 모빌리티 앞당긴다](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000967t.jpg)