|
아리바이오는 최근 미국 식품의약국(FDA)와 치매치료제 AR1001의 임상 2상 종료 미팅을 성공적으로 완료했다. 오는 7월 미국 FDA에 글로벌 3상 허가 신청과 함께 8월 완제의약품 제조 완료 및 12월 환자 투약을 계획하고 있다.
AR1001은 뇌혈관을 확장해 혈류를 개선하고 신경세포의 사멸 억제, 장기기억 형성 단백질과 뇌세포 증식 단백질의 활성화, 뇌의 독성 단백질을 제거하는 등 다중 작용 기전의 경구용 치매 치료제다. 미국 임상 2상을 통해 치매 진행 억제와 인지기능 향상 효과가 성공적으로 입증됐다.
또한 한국 신경과학회 교수 및 전문의와 알츠하이머 전문가 미팅을 열어 한국과 미국 치매 임상에 대한 토론, 글로벌 알츠하이머병 치료제 개발 현황, 미래 신약 전망 등 치매 치료제 개발에 대한 글로벌 정보를 공유할 예정이다. 연세대 대사성치매센터 등 치매 관련 한국 기관과 제약사 연구소도 방문할 계획이다.
그릴리 교수는 특히 지난해 11월 보스턴에서 열린 제 14차 알츠하이머병 임상시험 학회(CTAD)에서 AR1001 임상 2상 결과를 직접 발표해 주목을 받았다. 그릴리 교수는 “임상 2상에서 구강 투여 결과 AR1001은 상대적으로 안전하고 혈류, 뇌 장벽 투과성이 다른 치료제(PDE5억제제)에 비해 우수한 것으로 보인다” 며 ”뇌 혈류를 증가시키고 독성 단백질을 감소시키며, 신경 보호 효과 뿐만 아니라 잠재된 다른 효과도 기대된다”고 밝힌 바 있다.









![[포토]현세린,정확한 임팩트](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110100215t.jpg)
![[포토] '트릭 오어 트릿' 진행하는 바이든 대통령 부부](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103102211t.jpg)
![[포토] 송민혁 '이글 2개, 버디7개 잡은 날'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103100152t.jpg)
![[포토]치솟던 배춧값 대폭 하락…"물량 충분해"](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103101370t.jpg)
![[포토]삼성전자 반도체 영업익 4조](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103101369t.jpg)
![[포토]하모니카 연주가 이윤석의 연주](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103101230t.jpg)
![[포토]민통선 주민들 트랙터 시위](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103101122t.jpg)
![[포토] 서울시예산안 설명하는 오세훈 시장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103100890t.jpg)
![[포토] 벤틀리모터스코리아, '더 뉴 컨티넨탈 GT 스피드' 공개](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103100418t.jpg)
![[포토] 2024 서울 문화원 엑스포](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/10/PS24103001770t.jpg)
![[포토]최민경,버디 성공 볼인다](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110100243t.jpg)

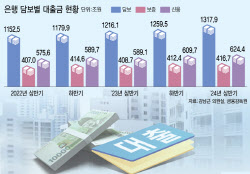
![[단독]대출 74%가 담보·보증대출…위험 피하는 은행](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110100154b.jpg)
![‘AI투자 확대 우려’에 나스닥 2.76%↓…금감원, 고려아연 유증 제동[뉴스새벽배송]](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/11/PS24110100413b.jpg)
