시선바이오머티리얼스(박희경 대표)는 13일 감염성 영아 난청 검사키트인 ‘유톱CMV디텍션키트’(U-TOP CMV Detection Kit)가 식품의약품안전처로부터 체외진단의료기기(3등급)로 품목허가를 받았다고 15일 밝혔다.
거대세포바이러스(CMV)는 전세계 성인의 60% 이상이 일생에 한번은 감염되는 포진바이러스 계열의 병원체로, 한번 감염되면 평생 체내에 잠복 상태로 존재하고 대체로 감염질환을 일으키지 않지만 태아감염의 경우 치명적인 질환을 유발할 수 있다. 산모가 CMV에 감염되면 태아의 약 40%가 수직감염돼 매년 신생아 150명당 1명꼴로 선천성 CMV 감염질환을 보인다. 이로 인해 유산, 영아의 난청·시각장애·소두증·성장지연·뇌성마비 등이 나타날 수 있다.
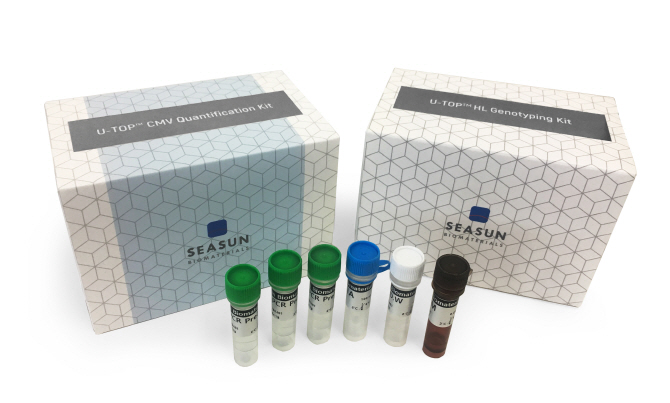
시선바이오는 이번 유톱CMV디텍션키트 출시로 선천성 난청 진단 플랫폼을 더욱 확고히 하게 됐다. 2016년 1월 품목허가를 받아 올해 7월부터 보험급여가 적용된 유전성 난청 유전자 검사 제품인 ‘유톱히어링로스유전자진단키트(U-TOP HL Genotyping Kit)가 최근 임상현장에서 빠르게 보급되면서 이번에 허가된 유톱CMV키트와의 통합검사를 통해 영아의 유전성·감염성 난청 진단이 모두 가능할 것으로 기대되기 때문이다.
박희경 대표는 “현재 신생아청각선별검사에 이용되는 유발이음향방사검사법과 청성뇌간반응검사법은 청력의 정도나 귀의 구조적 이상을 확인하는 검사로, 정확도가 부족하고 뚜렷한 원인 분석이 어려운 게 단점”이라며 “시선바이오의 두 가지 난청 키트는 검사가 신속·정확한 데 그치지 않고 선천성 난청의 대다수를 차지하는 유전성·감염성 난청 원인인자를 정밀하게 집어낼 수 있어 기존 검사의 한계를 보완할 수 있다”고 설명했다. 이어 “선천성 CMV 감염 여부는 출생 후 3주 이내 검사해야 정확한 결과를 알 수 있으나 일부 영아는 출생 수개월 후에 난청 증상이 발현되는 경우가 있어 증상이 없더라도 검사할 필요가 있다”고 덧붙였다.
|


![월드컵까지 따냈다...스포츠산업 '생태계 파괴자' 된 빈살만[글로벌스트롱맨]](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/11/PS23110500115t.jpg)

![[포토] 폭염 속 휴식취하는 건설 근로자](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/08/PS23080100718t.jpg)






![[포토]국군장병 취업박람회 인재 채용](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900871t.jpg)
![[포토]멘토들 강연 경청하는 오세훈 시장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900762t.jpg)
![[포토]KT그룹, AI로 미디어·콘텐츠 산업 '가속도'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900526t.jpg)
![[포토] 한우자조금, "한우로 행복하세요~"](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900479t.jpg)
![[포토]'국민의힘 당선자 총회'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900379t.jpg)
![[포토] '미래전략포럼' 개회사하는 박재완 위원장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900377t.jpg)
![[포토]'최고위 참석하는 이재명 대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042900358t.jpg)
![[포토] 임성재의 우승 본능](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042800425t.jpg)
![[포토]이정민 '구름 갤러리와 함께 입장'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042800395t.jpg)
![[포토]파워에이드와 함께 다 마신 페트병 재활용 하세요!](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042800282t.jpg)
