코젠바이오텍, 씨젠(096530), 솔젠트, SD바이오센서, 바이오세움에 이어 국내에서는 6번째 긴급사용 승인이다.
|
바이오코아는 이번에 질본 긴급사용 승인마저 획득함으로써 국내 내수시장 진출도 병행해 나갈 계획이다. 현재 승인 대기 중인 미국 식품의약국(FDA) 긴급사용 승인(EUA) 역시 임박함에 따라 미국 시장 진출을 본격화할 예정이다.
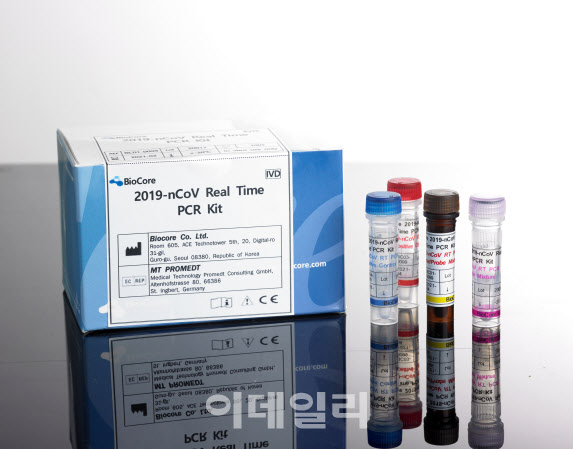
바이오코아 코로나19 진단키트는 세계보건기구(WHO) 가이드라인에서 권고하는 ‘실시간 유전자 증폭 기법’(RT-PCR) 방식으로, N과 RdRp 두 가지 유전자 부위를 한 개의 튜브로 증폭해 사용 편의성을 높였다. 계속해서 발생되고 있는 코로나19 변이는 위음성(실제 양성임에도 음성으로 오판되는 사례) 원인이 될 수 있는데, 변이 여부와 상관없이 검출할 수 있도록 고안해 특이도를 제고했다.
한성희 바이오코아 생명공학사업본부장(상무)은 “각 해외 국가 및 정부 부처로부터 쇄도하는 공급 요청에 대응하기 위해 생산량을 대폭 확대하고 있다”며 “미(美) FDA에 긴급사용승인 신청을 하고 승인을 기다리고 있다”고 설명했다.


![월드컵까지 따냈다...스포츠산업 '생태계 파괴자' 된 빈살만[글로벌스트롱맨]](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/11/PS23110500115t.jpg)

![[포토] 폭염 속 휴식취하는 건설 근로자](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/08/PS23080100718t.jpg)






![[포토]노동해방하는 그날을 위하여](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24050100452t.jpg)
![[포토]경기 침체에 폐업 급증, '한산한 주방거리'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24050100378t.jpg)
![[포토] GS칼텍스 매경오픈 공식 포토콜 '많이 찾아와 주세요'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24050100074t.jpg)
![[포토]가정의달 5월, '외식물가 가파르게 상승 중'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24050100329t.jpg)
![[포토]맥도날드, '반년만에 또 가격 인상...평균 2.8% 인상'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24050100325t.jpg)
![[포토]해외동포들과 티타임 갖는 한덕수 국무총리](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24050100303t.jpg)
![[포토] 시흥 고가차로 공사장서 교량 상판 붕괴](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043001298t.jpg)
![[포토]코스피, 질주하는 테슬라 증시 훈풍](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000818t.jpg)
![[포토] 꽃처럼 아름다워](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000766t.jpg)
![[포토]국방 AI정책방향 소개하는 이영빈 기획조정실장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24043000623t.jpg)
