|
후성유전을 결정하는 대표적 인자인 크로마틴 구성 히스톤 단백질의 화학적 변성은 세포 분화와 개체 발생 및 다양한 인간 질환의 진행과 밀접한 관련성이 있다.
특히 크로마틴을 구성하는 4개 대표 히스톤 단백질(H2A, H2B, H3, H4) 중 히스톤 H3의 효소에 의한 촉매반응(메틸화)은 유전체의 발현, 유전체 안정성 유지 및 재조합 조절 등과 같은 핵심적인 유전체 기능 조절에 깊이 관여하는 것으로 알려져 있다.
히스톤 H3의 비정상적인 변성은 질환 관련 유전자의 발현 이상을 일으켜서 암과 같은 난치성 질환을 유발하거나 항암치료 저항성을 야기하는 등의 악성 진행을 촉진할 수 있다.
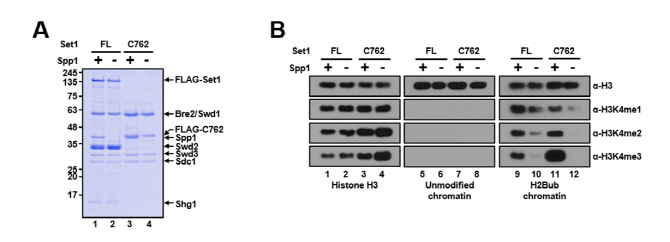
연구팀은 세포에서 직접 분리한 히스톤 단백질 H3의 촉매반응(메틸화)을 조절하는 효소와 생화학적으로 순수하게 재구성한 크로마틴을 이용해 세포 내에서 일어나는 히스톤 단백질 변성을 시험관 내에서 재현하고 이의 분석을 통해 히스톤 단백질의 작용원리를 규명했다. 연구에 사용된 크로마틴을 이용한 시험관 내 히스톤 단백질 변성 반응 유도는 기술적 어려움으로 인해 세계적으로도 구현 가능한 실험실이 소수에 불과하다.
공동연구책임자인 김정애 박사는 “이 연구 성과는 유전체 기능 조절에 핵심적인 H3 메틸화라는 후성유전인자를 가역적으로 조절할 수 있는 표적을 규명한 것”이라며 “H3 메틸화 제어를 통해 줄기세포 분화나 암세포 분화 및 역분화를 통해 조절되는 다양한 질환 치료제 개발에 큰 기여를 할 것으로 기대된다”고 말했다.
한국생명공학연구원 유전체맞춤의료연구단의 김정애 박사팀과 한국과학기술원의 김재훈 교수팀이 수행한 이번 연구는 한국연구재단이 추진하는 신진연구자지원사업(김정애) 및 삼성전자 미래기술육성재단의 기초과학 지원사업(김재훈)의 지원으로 수행됐다. 생물학 분야의 국제 저널인 핵산지(Nucleic Acids Research) 지난해 11월 30일자 판에 ‘Breakthrough Article’로 선정·게재됐다.

![월드컵까지 따냈다...스포츠산업 '생태계 파괴자' 된 빈살만[글로벌스트롱맨]](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/11/PS23110500115t.jpg)

![[포토] 폭염 속 휴식취하는 건설 근로자](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/08/PS23080100718t.jpg)






![[포토]성년의날, 덕수궁 돌담길서 전통셩년례 열려](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051900274t.jpg)
![[포토]물놀이하며 더위 잊어요!](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051900249t.jpg)
![[포토]박현경 '버디 성공 승리했어요'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051900379t.jpg)
![[포토]개혁신당 전당대회, '인사하는 당 대표 후보들'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051900216t.jpg)
![[포토]주유소 기름값 하락](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051900204t.jpg)
![[포토]'다양한 음식 맛보세요'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051900192t.jpg)
![[포토] 최경주 '우승은 전설도 춤추게 한다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051900414t.jpg)
![[포토] 최경주 '리빙 레전드의 클래스'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051800445t.jpg)
![[포토]유효주 '핀을 잡고 라인을 살핀다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051800234t.jpg)
![[포토]두산 매치플레이에서 공기청정기 선보인 아이큐에어](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051700873t.jpg)
![[단독]EU, 韓정부에 "전기차 보조금 기준 예측 가능성 떨어져…손봐달라"](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051900339t.jpg)
![[포토]매치퀸 박현경 '힘들었지만 최고의 하루'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/05/PS24051900488t.jpg)