뉴스 검색결과 10,000건 이상

- 고형암 시장 누빌 암 치료 백신 개발사 TOP4, 개발 현황은?
- [이데일리 김진호 기자] 2028년을 전후로 고형암 시장을 두드릴 암 치료 백신 신약의 등장이 예고되고 있다. 글로벌 3상 이상 단계에 진입한 암 치료 백신 후보물질을 확보한 주요 기업은 총 4곳이다. 미국 모더나와 셀라스 라이프 사이언스(셀라스), 프랑스 OSE이뮤노테라퓨틱스, 독일 IO 바이오테크 등이 그 주인공이다. 국내에서는 애스톤사이언스가 이들을 뒤쫓기 위해 pDNA 기반 암 치료 백신 후보물질의 글로벌 임상 개발을 서두르고 있다. 미국 모더나와 셀라스 라이프 사이언스(셀라스), 프랑스 OSE이뮤노테라퓨틱스, 독일 IO 바이오테크 등 4곳이 암 치료 백신 시장을 이끌 유력 후보기업으로 떠오르고 있다.(제공=게티이미지, 각사)암 치료 백신은 암 진단을 받은 환자에게 해당 암에 대한 항원을 투입해 면역시스템의 활성화를 유도하는 의약품이다. 이는 곧 2~4기 이상 후기 난치암 환자에서 신체의 면역능력을 높여, 암의 재발을 막기 위한 용도로 쓰일 수 있는 셈이다. 각국의 기업들은 mRNA부터 펩타이드, pDNA 등 다양한 기술에 기반한 암 치료 백신 후보물질을 발굴해 개발하는 중이다.27일 제약바이오 업계에 따르면 모더나를 비롯한 주요 암 치료 백신 개발사들은 2028년~2030년경 그 시장이 크게 형성될 것으로 예고하고 있다. 현재 개발 중인 암 치료 백신 신약들이 이때부터 상용화 가도에 오를 수 있다는 얘기다.암 치료 백신 개발에 있어 가장 앞선 곳은 모더나와 셀라스, OSE이뮤노테라퓨틱스, IO바이오테크 등 4곳이다. 먼저 모더나는 지난해 8월 흑색종 환자를 대상으로 mRNA 기반 암 치료 백신 후보물질 ‘mRNA-4157’과 미국 머크(MSD)의 면역항암제 ‘키트루다’ 등을 병용하는 임상 3상을 개시했다. 모더나에 따르면 mRNA-4157과 키트루다 병용요법의 임상 2b상에서 흑색종 환자의 사망 위험을 키트루다 단독요법 대비 65% 감소시킨 것으로 분석됐다. 이에 더해 지난 4월 회사는 mRNA-4157과 키트루다의 두경부편평세포암 대상 임상 1상 중간 결과에서를 발표했다. 여기서 객관적 반응률이 27%대로 확인되면서 적응증 확대 가능성도 점쳐지고 있다.셀라스가 개발 중인 펩타이드 기반 암 치료 백신 후보물질 ‘GALINPEPIMUT-S’(GPS)는 급성 림프구성 백혈병(AML) 대상 임상 3상을 진행 중이다. 이외에도 회사에 따르면 △2차 또는 3차 치료 단계에서 난소암 대상 키트루다와 GPS 병용요법 △악성 흉막 종피종(MPM) 대상 GPS 단독요법 등의 임상 2상을 완료했고, 난소암과 MPM 등 각 적응증 대상 GPS와 면역항암제 ‘옵디보’(성분명 니볼루맙) 병용요법도 임상 1상이 종료된 것으로 확인됐다. 또다른 암 치료 백신 전문 OSE 이뮤노테라퓨틱스는 자체 발굴한 ‘테도피’에 대해 면역항암제 치료 전력이 있는 비소세포폐암 대상 글로벌 확증 임상 3상을 진행하고 있다. 해당 물질의 탐색 임상에서 대조군 대비 비소세포폐암 환자의 사망 위험을 41%가량 낮춘 것으로 확인되면서 유력한 암 치료 백신 신약 후보물질로 떠올랐다 지난 2019년 종근당(185750)이 테도피의 국내 개발 및 판매 권리를 OSE이뮤노테라퓨틱스로부터 기술이전받은 바 있다.마지막 주자로 IO바이오엔테크는 자사의 ‘IO102-IO103’에 대해 흑색종(임상 3상) 및 전이성 비소세포폐암(임상 2상)등의 연구를 병행하고 있다.암 치료 백신 개발 업계 한 관계자는 “모더나와 같은 곳이 선제적으로 암 치료 백신 개발에 성공하는 선례를 창출해야 한다”며 “이를 통해 해당 분야에 대한 인식 제고와 투자 활성화가 이뤄진다면 후발주자들의 개발에도 훈풍으로 작용할 것”이라고 말했다. 이어 “다양한 암종이 있기 때문에 후발주자도 개발에 성공하면, 시장성은 얼마든지 확보할 수 있을 것”이라고 말했다.애스톤사이언스는 pDNA 기반 암 치료 백신 후보물질 AST-301에 대해 유방암 대상 글로벌 임상 2상을 진행하고 있다.(제공=애스톤사이언스)국내 기업 중 암 치료 백신 개발에서 가장 앞선 곳은 애스톤사이언스다. 회사는 pDNA 방식의 후보물질 3종(AST-301, AST-302, AST-201)과 펩타이드 방식 1종(AST-021p) 등 4종의 임상 단계 후보물질을 확보하고 있다. 애스톤사이언스에 따르면 △HER2 타깃용 AST-301(미국 및 호주 등 유방암 대상 글로벌 임상 2상 진행) △HER2와 IGFBP-2, IFG-IR 등 다중 타깃용 ‘AST-302’(미국 등 글로벌 1상 완료) △IGFBP2 타깃용 난소암 대상 ‘AST-201’(국내 1상 완료) △HSP90 타깃용 AST-021p(국내 임상 1상 완료) 등의 개발 절차를 밟고 있다. 특히 이중 AST-301은 pDNA 방식의 암 치료 백신 중 가장 빠른 2028년 상용화를 목표로 개발되고 있다.한편 글로벌 시장조사기관 프리시던스 리서치에 따르면 글로벌 항암신 시장은 2022년 91억2000만달러(한화 약 12조4800억원)에서 2032년 269억8000만달러(36조9300억원)로 10년 새 약 3배 수준으로 커질 것으로 전망되고 있다.다만 이 같은 항암백신 시장의 80~85%는 머크의 자궁경부암 예방 백신 ‘가다실’ 제품군을 필두로 하는 암 예방 백신 시장이 될 것으로 예측된다. 앞서 언급한 암 치료 백신 후보물질들이 상용화에 성공할 경우 그 나머지 비율 만큼의 시장을 형성할 것으로 분석되고 있다.

- [아는 것이 힘]변비 있다면 '알츠하이머 치매' 위험 2배 높아져
- [이데일리 이순용 기자] 장과 뇌 건강 사이의 관계를 설명하는 개념이 관심을 끌고 있다. 장을 ‘제2의 뇌’라고 보는 ‘장뇌축(gut-brain axis)’ 이론에 따르면 장내 미생물 균형이 깨지거나 장 건강이 악화되면 뇌 기능과 감정 상태에도 영향을 미칠 수 있다. 특히 치매와 같은 퇴행성 뇌질환과도 관련이 있는 것으로 나타났다.‘장뇌축’ 이론은 장과 뇌의 상호작용을 설명하는 것으로, 장내 미생물이 뇌와 장을 연결하는 신호 전달 역할을 한다는 이론이다. 장내 세균의 불균형은 염증과 스트레스를 증가시키고, 신경전달물질의 생성과 조절에 영향을 줄 수 있어 우울, 불안, 인지기능저하와 관련될 수 있다. 또한 뇌신경 물질 중 편안함을 느끼게 하는 세로토닌을 포함한 많은 것들이 장내 미생물에 의해 만들어진다.‘저널 오브 어드밴스트 리서치(Journal of Advanced Research)’에 게재된 광주과학기술원(GIST), 경희의료원 디지털헬스센터의 기초-임상 융합연구에서는 장 운동성 저하와 알츠하이머병 사이의 인과관계가 규명됐다.알츠하이머 마우스 모델에 지사제의 일종인 ‘로페라미드’를 투여한 결과, 뇌 내의 아밀로이드 베타 단백질과 뇌 내 면역세포가 유의미하게 증가했고 기억력 저하 등 병리현상이 나타나는 것으로 확인했다. 또한 약 313만명의 한국인과 약 438만명의 일본인에서 변비가 있는 환자의 경우, 그렇지 않은 환자에 비해 알츠하이머병의 위험비가 한국 코호트에서는 2.04배, 일본 코호트에서는 2.82배 높은 경향을 확인했다.흔히 알고 있는 알츠하이머병은 원인 미상의 신경퇴행성 질환으로 전체 치매의 절반 이상을 차지한다. 두뇌의 수많은 신경세포가 서서히 쇠퇴하면서 뇌 조직이 소실되고 뇌가 위축되는 질환이다. 초기에는 최근 일에 대한 기억력에서 문제를 보이다가 점차 언어기능, 판단력 등 다른 인지기능의 이상을 동반하게 된다.알츠하이머는 일반적으로 8 ~10년에 걸쳐 서서히 진행된다. 인지지능 저하뿐만 아니라 망상, 우울, 불안, 초조, 수면장애 등 정신행동증상에 대한 치료도 중요하다. 말기 치매의 경우 신경학적 증상과 기타 신체적 합병증이 생겨 독립적인 생활이 불가능하며 대소변실금, 욕창, 폐렴, 요로감염증 등 합병증으로 사망하는 경우가 많다.세란병원 신경과 이은주 과장은 “변비가 있으면 치매 위험이 2배 이상 높아질 수 있다는 연구는 우리 몸의 장과 뇌가 긴밀하게 상호작용한다는 주장을 뒷받침한다”며 “장 운동을 느리게 하는 지사제를 복용한 실험쥐는 알츠하이머 환자 뇌에서 발견되는 아밀로이드 베타 단백질이 증가했다”고 설명했다. 이어 “실제 환자들의 데이터를 살펴보면 장 운동 기능이 떨어지면 알츠하이머병이 악화될 수 있음을 알 수 있다”며 “치매 환자의 대부분을 차지하는 알츠하이머병은 인지 기능 장애가 서서히 일어나기 때문에 사전에 악화를 막는 것이 중요하다”고 강조했다.
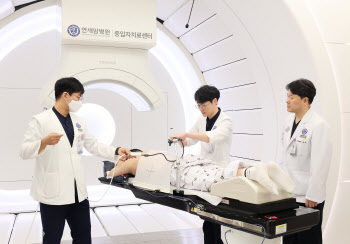
- 췌장암과 간암 3기 환자, 회전형 중입자치료 시작
- [이데일리 이순용 기자] 난치암으로 불리는 췌장암, 간암 치료에 중입자치료가 시작됐다.연세암병원은 28일 췌장암 3기 환자 김모씨(남 ·47세)를 대상으로 회전형 중입자치료기 가동을 시작했다고 밝혔다. 치료는 주 4회씩 총 12회로 3주간 진행된다.간암 3기 진단을 받은 이모씨(여 ·73세)도 같은 날 중입자치료를 시작했다. 총 4회 조사를 받는 이씨의 치료는 일주일 만에 끝난다.김씨는 2021년 췌장암 3기 진단을 받고 수술이 불가한 상태로 연세암병원에서 항암약물치료를 시작했다. 진단 당시 종양이 복부 혈관을 둘러싸고 있어 24차례 항암약물치료를 시행했으나 암이 더 진행됐다. 이어 스텐트를 삽입해 황달 증상을 조절한 뒤 약제를 바꿔 항암약물치료를 지속하던 중 중입자치료를 결정했다.췌장암의 5년 생존율은 10%에 불과하다. 하지만 일본 방사선의학 종합연구소(QST)에 따르면 병기가 진행돼 수술이 불가한 췌장암 환자의 경우 항암제와 중입자치료를 병행했을 때, 2년 국소제어율이 80%까지 향상됐다는 결과가 있다. 국소제어율은 치료받은 부위에서 암이 재발하지 않는 확률로 특정 부위(국소, 局所)를 타깃하는 중입자치료에 있어 치료 성적을 알 수 있는 주요 지표다. 중입자치료 후 2년 생존율이 56%라는 성적도 나오고 있어 우수한 치료 효과가 입증됐다.2022년 간암 3기 판정을 받은 이씨는 수술을 받았지만 2023년 재발했다. 이후 수술을 한 번 더 받고 항암치료를 진행했으나 2024년 다시 재발했다는 소견을 듣고 면역항암제를 복용하던 중 중입자치료를 받기 위해 연세암병원을 찾았다.간암은 방사선치료가 까다롭다. 신경세포가 적은 탓에 통증을 잘 느끼지 못해 발견이 늦어 애초에 병기가 많이 진행된 상태에서 진단받는 데다, 간경화 등으로 간 기능이 저하돼 방사선으로 인한 간독성 위험이 크다. 중입자치료는 정상 세포는 피하고 암세포에만 고선량 방사선을 집중 타깃하는 특성으로 부작용은 줄이되 치료 효과는 높일 수 있다.일본 군마대학병원에서 중입자치료를 받은 간암 환자의 2년 국소제어율은 92.3%에 달했다. QST의 임상연구에서는 5년 국소제어율 81%를 기록했다. 특히 종양의 크기가 4cm 이상으로 큰 경우에도 2년 국소제어율이 86.7%였고, 2년 생존율은 68.3%로 높았다.중입자치료는 필요 시 항암치료 등 기존 치료와 함께 사용해 치료 효과를 높일 수 있다. 특히 췌장암, 간암과 같이 발견이 늦어 병기가 진행된 채로 진단돼 수술이 어려운 경우 환자의 상태에 따라 항암치료 등으로 암 크기를 줄인 뒤 중입자치료를 이어가는 형식이다.연세암병원은 고정형치료기 1대와 회전형치료기 2대를 보유하고 있다. 치료기는 탄소입자의 조사 각도에 따라 두 종류로 나뉜다. 수평으로 고정된 각도에서 조사하는 고정형치료기는 좌측과 우측에서 입자선을 조사하기에 적절한 전립선암을 대상으로 한다. 장기가 호흡과 중력에 따라 움직이고 주변에 다른 장기가 있어 다양한 각도로 조사해야 하는 췌장암, 간암, 폐암 등에는 회전형치료기를 사용한다.본격적으로 가동을 시작한 회전형치료기는 치료기 안에 환자가 누우면 가장 적합한 각도로 치료기가 회전해 설계된 치료계획에 따라 암세포를 타격한다. 360도 어느 각도에서도 조사가 가능해짐에 따라 해부학적 위치에 맞게 정상 장기에 대한 보호와 종양에 대한 치료 정확도를 최대화할 수 있다.금웅섭 연세암병원 방사선종양학과 교수는 “췌장암과 간암은 주변에 정상 장기가 많고 발견이 늦는 경우가 잦아 수술이 어려운 상황이 많지만, 중입자치료는 이때도 효과를 기대할 수 있다”며 “기존의 항암치료와 새로운 중입자치료의 조화를 잘 이뤄서 최고의 치료 효과를 낼 수 있도록 최선의 노력을 하겠다”라고 말했다.금웅섭 교수와 의료진이 정확한 치료를 위해 중입자 치료장비를 조정하고 있다.