|
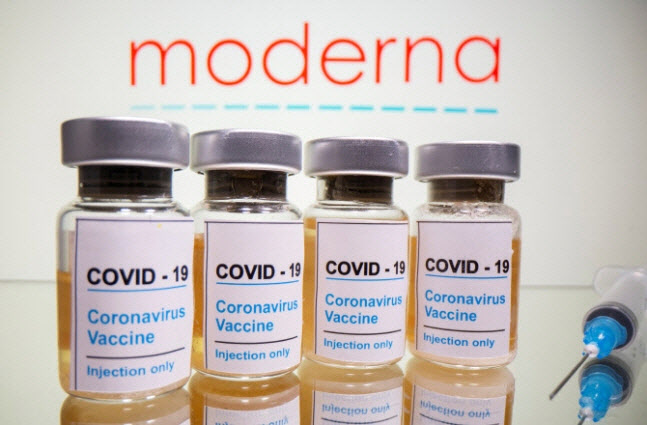
지난달 30일(현지시간) CNBC 등에 따르면 모더나는 자사의 백신이 94.1%의 효과가 있는 것으로 나타났다는 3상 임상시험 최종 분석 결과를 바탕으로 이날 미국 식품의약국(FDA)과 유럽의약품청(EMA)에 긴급 사용 승인을 신청했다. 3상 임상시험에는 3만여명이 참가했다.
모더나의 승인 신청은 화이자에 이어 두 번째다. 두 회사는 코로나19 백신을 신기술인 ‘메신저 리보핵산’(mRNA·전령RNA) 방식으로 개발했다.
스테판 반셀 모더나 최고경영자(CEO)는 “이번 분석은 코로나19를 예방할 수 있는 백신의 능력을 확인해 주고 있다”며 “우리는 이 백신이 코로나19에 따른 질병과 입원, 사망을 예방하는데 도움을 줄 것이라고 믿는다”고 말했다.
FDA는 빠르게 승인 절차를 밟을 것으로 보인다. 12월17일 모더나 백신 심의를 위한 회의를 열 것으로 알려졌다. 앞서 FDA를 관할하는 보건복지부의 앨릭스 에이자 장관은 “FDA가 가능한 한 빠르게 화이자와 모더나의 백신을 승인할 것”이라고 했다. 이럴 경우 연내 접종이 가능할 전망이다.
이날 모더나 주가는 백신 희소식에 폭등했다. 전날 대비 20.24% 오른 주당 152.74달러에 거래를 마쳤다.


![월드컵까지 따냈다...스포츠산업 '생태계 파괴자' 된 빈살만[글로벌스트롱맨]](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/11/PS23110500115t.jpg)

![[포토] 폭염 속 휴식취하는 건설 근로자](https://image.edaily.co.kr/images/Photo/files/NP/S/2023/08/PS23080100718t.jpg)






![[포토]김희지 '핀 주변을 살핀다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042500654t.jpg)
![[포토]2024 이데일리 금융투자대상 금융투자 부분 수상자들](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042501046t.jpg)
![[포토]'서울외신기자클럽 기자간담회 참석하는 이준석 대표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042500759t.jpg)
![[포토]쾌적한 비행을 위해 봄맞이 세척](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042500578t.jpg)
![[포토] '법의 날' 축사하는 이종석 헌법재판소장](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042500502t.jpg)
![[포토]'기자회견 기다리는 황운하'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042500358t.jpg)
![[포토]정책조정회의, '모두발언하는 홍익표'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042500272t.jpg)

![[포토]이주호 사회부총리, 40개 의대 총장 간담회…"학생·교수 복귀 총력"](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042400781t.jpg)
![[포토] '인구감소 시대의 부동산 정책 및 시장 영향'](https://image.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042400618t.jpg)
![[포토]김희지 '위로 올라간다'](https://spnimage.edaily.co.kr/images/Photo/files/NP/S/2024/04/PS24042500664t.jpg)
